Kamis, 28 Maret 2013
PENENTUAN BILANGAN ASAM PADA MINYAK/LEMAK
Penentuan bilangan asam dipergunakan untuk mengukur jumlah asam lemak bebas yang terdapat dalam minyak atau lemak. Besarnya bilangan asam tergantung dari kemurnian dan umur dari minyak atau lemak tersebut.
Analisa minyak dan lemak yang umumnya banyak dilakukan dalam bahan makanan adalah penentuan sifat fisik maupun kimiawi yang khas mencirikan sifat minyak tertentu sehingga dapat dianalisa dengan bilangan asam pada suatu sampel.
Bilangan asam adalah ukuran dari jumlah asam lemak bebas, serta dihitung berdasarkan berat molekul dari asam lemak atau campuran asam lemak. Bilangan asam dinyatakan sebagai jumlah milligram KOH yang digunakan untuk menetralkan asam lmak bebas yang terdapat dalam 1 gram minyak atau lemak.
Bilangan asam yang besar menunjukkan asam lemak bebas yang besar pula, yang berasal dari hidrolisa minyak atau lemak, ataupun karena proses pengolahan yang kurang baik. Makin tinggi bilangan asam, maka makin rendah kualitasnya.
Asam lemak bebas merupakan hasil degradasi/ deesterifikasi/ hidrolisislemak yang dapat menunjukkan kualitas bahan makanan mulai menurun. Reaksihidrolisis lemak adalah sebagai berikut:
Trigiserida + 3 H2O --> asam lemak + gliserol
Banyaknya asam lemak bebas yang terdapat dalam suatu lemak atauminyak dinyatakan dengan bilangan asam. Bilangan asam merupakan jumlahmiligram KOH yang diperlukan untuk menetralkan asam lemak bebas yangterdapat dalam satu gram lemak atau minyak. Penetapan bilangan asam dilakukan dengan cara melarutkan ekstrak lemak dalam alkohol netral panas danditambahkan beberapa tetes fenolftalein sebagai indikator. Alkohol netral panasdigunakan sebagai pelarut netral supaya tidak mempengaruhi pH karena titrasi inimerupakan titrasi asam basa. Alkohol dipanaskan untuk meningkatkan kelarutanasam lemak. Reaksi yang terjadi merupakan reaksi asam dengan basa yang menghasilkan garam. Reaksinya adalah sebagai berikut:
C17H29COOH + KOH --> C17H29COOK + H2O
PENETAPAN KADAR LEMAK METODE SOXHLET
Lemak merupakan bagian dari lipid yang mengandung asam lemak jenuh bersifat padat. Lemak merupakan senyawa organik yang terdapat di alam serta tidak larut dalam air, tetapi larut dalam pelarut organik nonpolar, misalnya dietil eter (C2H5OC2H5), kloroform (CHCl3), benzena, hexana dan hidrokarbon lainnya. Lemak dapat larut dalam pelarut tersebut karena lemak mempunyai polaritas yang sama dengan pelarut.
Dalam mengetahui kadar lemak yang terdapat di bahan pangan dapat dilakukan dengan mengekstraksi lemak. Namun mengekstrak lemak secara murni sangat sulit dilakukan, sebab pada waktu mengekstraksi lemak, akan terekstraksi pula zat-zat yang larut dalam lemak seperti sterol, phospholipid, asam lemak bebas, pigmen karotenoid, khlorofil, dan lain-lain. Pelarut yang digunakan harus bebas dari air (pelarut anhydrous) agar bahan-bahan yang larut dalam air tidak terekstrak dan terhitung sebagai lemak dan keaktivan pelarut tersebut menjadi berkurang.
Sifat-sifat dari lemak dapat diidentifikasi dengan beberapa metode Terdapat dua metode untuk mengekstraksi lemak yaitu metode ekstraksi kering dan metode ekstraksi basah. Metode kering pada ekstraksi lemak mempunyai prinsip bahwa mengeluarkan lemak dan zat yang terlarut dalam lemak tersebut dari sampel yang telah kering benar dengan menggunakan pelarut anhydrous. Keuntungan dari dari metode kering ini, praktikum menjadi amat sederhana, bersifat universal dan mempunyai ketepatan yang baik. Kelemahannya metode ini membutuhkan waktu yang cukup lama, pelarut yang digunakan mudah terbakar dan adanya zat lain yang ikut terekstrak sebagai lemak. Pada praktikum penetapan kadar lemak ini digunakan metode ekstraksi kering yaitu metode Soxhlet.
Tujuan
Praktikum penetapan lemak kasar dan komponen lipid dilakukan dengan tujuan agar praktikan dapat mengetahui kadar lemak yang terkandung dalam suatu bahan pangan. Metode yang digunakan tergolong dalam metode ekstraksi kering yaitu metode Soxhlet
METODE SOXHLET
Metode Soxhlet termasuk jenis ekstraksi menggunakan pelarut semikontinu. Ekstraksi dengan pelarut semikontinu memenuhi ruang ekstraksi selama 5 sampai dengan 10 menit dan secara menyeluruh memenuhi sampel kemudian kembali ke tabung pendidihan. Kandungan lemak diukur melalui berat yang hilang dari contoh atau berat lemak yang dipindahkan. Metode ini menggunakan efek perendaman contoh dan tidak menyebabkan penyaluran. Walaupun begiru, metode ini memerlukan waktu yang lebih lama daripada metode kontinu.
Prinsip Soxhlet ialah ekstraksi menggunakan pelarut yang selalu baru yang umumnya sehingga terjadi ekstraksi kontiyu dengan jumlah pelarut konstan dengan adanya pendingin balik. Soxhlet terdiri dari pengaduk atau granul anti-bumping, still pot (wadah penyuling, bypass sidearm, thimble selulosa, extraction liquid, syphon arm inlet, syphon arm outlet, expansion adapter, condenser (pendingin), cooling water in,dan cooling water out .
Langkah-langkah dalam metode Soxhlet adalah :
Menimbang tabung pendidihan ; menuangkan eter anhydrous dalam tabung pendidihan, susun tabung pendidihan, tabung Soxhlet, dan kondensator ; ekstraksi dalam Soxhlet ; mengeringkan tabung pendidihan yang berisi lemak yang terekstraksi pada oven 1000C selama 30 menit ; didinginkan dalam desikator lalu ditimbang.
Sampel yang sudah dihaluskan, ditimbang 5 sampai dengan 10 gram dan kemudian dibungkus atau ditempatkan dalam “Thimble” (selongsong tempat sampel) , di atas sampel ditutup dengan kapas. Pelarut yang digunakan adalah petroleum spiritus dengan titik didih 60 sampai dengan 80°C. Selanjutnya, labu kosong diisi butir batu didih. Fungsi batu didih ialah untuk meratakan panas. Setelah dikeringkan dan didinginkan, labu diisi dengan petroleum spiritus 60 – 80°C sebanyak 175 ml. Digunakan petroleum spiritus karena kelarutan lemak pada pelarut organik. Thimbleyang sudah terisi sampel dimasukan ke dalam Soxhlet. Soxhlet disambungkan dengan labu dan ditempatkan pada alat pemanas listrik serta kondensor . Alat pendingin disambungkan dengan Soxhlet. Air untuk pendingin dijalankan dan alat ekstraksi lemak kemudian mulai dipanaskan.
Ketika pelarut dididihkan, uapnya naik melewati Soxhlet menuju ke pipa pendingin. Air dingin yang dialirkan melewati bagian luar kondensor mengembunkan uap pelarut sehingga kembali ke fase cair, kemudian menetes ke thimble. Pelarut melarutkan lemak dalam thimble, larutan sari ini terkumpul dalam thimble dan bila volumenya telah mencukupi, sari akan dialirkan lewat sifon menuju labu. Proses dari pengembunan hingga pengaliran disebut sebagai refluks. Proses ekstraksi lemak kasar dilakukan selama 6 jam. Setelah proses ekstraksi selesai, pelarut dan lemak dipisahkan melalui proses penyulingan dan dikeringkan.
Faktor yang Memengaruhi Kadar Lemak
Faktor-faktor yang memengaruhi laju ekstraksi adalah tipe persiapan sampel, waktu ekstraksi, kuantitas pelarut, suhu pelarut, dan tipe pelarut. Dibandingkan dengan cara maserasi, ekstraksi dengan Soxhlet memberikan hasil ekstrak yang lebih tinggi karena pada cara ini digunakan pemanasan yang diduga memperbaiki kelarutan ekstrak. Makin polar pelarut, bahan terekstrak yang dihasilkan tidak berbeda untuk kedua macam cara ekstraksi. Fenolat total yang tertinggi didapatkan pada proses ekstraksi menggunakan pelarut etil asetat. Sifat antibakteri tertinggi terjadi pada ekstrak yang diperoleh dari ekstraksi menggunakan pelarut etil asetat untuk ketiga macam bakteri uji Gram-positif. Semua ekstrak tidak menunjukkan daya hambat yang berarti pada semua bakteri uji Gram-negatif.
Crackers
Crackers adalah jenis biskuit yang terbuat dari adonan keras melalui proses fermentasi atau pemeraman, berbentuk pipih yang mengarah kepada rasa asin dan renyah, serta bila dipatahkan penampang potongannya berlapis-lapis. Crackers tanpa pemanis merupakan tipe yang paling populer yang dapat dikonsumsi sebagai pengganti roti dan penggunaanya lebih luas sebagai makanan diet. Ciri-ciri crackersyang baik adalah tekstur yang renyah, tidak keras apabila digigit, tidak hancur, dan mudah mencair apabila dikunyah. Bahan-bahan yang digunakan dalam pembuatancrackers dapat dibagi menjadi dua bagian yaitu bahan-bahan yang berfungsi sebagai pengikat dan bahan pelembut tekstur. Bahan pengikat atau pembentuk adonan yang kuat adalah tepung terigu, air, dan garam, sedangkan bahan-bahan yang berfungsi sebagai pelembut tekstur adalah gula, mentega, dan leavening agent (baking powder)sebagai bahan pengembang.
Pelarut Heksana
n-Heksana adalah bahan kimia yang terbuat dari minyak mentah. Normal heksana tidak berwarna dan memiliki bau yang tajam. Bahan ini mudah terbakar dan uapnya bersifat eksplosif. Kebanyakan heksana digunakan pada industri sebagai pelarut. Pelarut yang menggunakan n-heksana bisanya digunakan untuk mengestrak minyak sayuran dari hasil pertanian, seperti kedelai. Pelarut ini juga digunakan sebagai agen pembersih pada percetakan, tekstil, furniture, dan industri pembuatan sepatu. Heksana larut hanya pada air. Kebanyakan n-heksana yang tumpah di air akan mengapung ke permukaan dimana heksana akan menguap ke udara.
Senin, 18 Maret 2013
KARBOHIDRAT
A. Pengertian Karbohidrat
Karbohidrat merupakan salah satu bahan makanan yang penting dan tersebar luas dalam jaringan binatang maupun tumbuh-tumbuhan. Karbohidrat adalah senyawa yang memiliki rumus umum Cn(H2O)m. Dalam karbohidrat terdapat gugus fungsional yaitu aldehid (polihidroksialdehid) dan keton (polihidroksiketon). Fungsi karbohidrat yaitu sebagai sumber energi dan penyusun sel tumbuhan. Karbohidrat terbentuk dari hasil fotosintesis tumbuhan.
H2O + CO2 à (C6H12O5)n
+ O2
B. Klasifikasi Karbohidrat
1. Berdasarkan Gugus Fungsi Utama
2. Berdasarkan Jumlah Monomer Penyusunnya :
- Aldosa (Polihidroksialdehid) : Karbohidrat yang memiliki gugus fungsi aldehid.
- Ketosa (Polihidroksiketon) : Karbohidrat yang memiliki gugus fungsi keton.
2. Berdasarkan Jumlah Monomer Penyusunnya :
- Monosakarida
a. Monosakarida berdasarkan jumlah atom C :
- Jumlah atom C = 3 --> Triosa
- Jumlah atom C = 4 --> Tetrosa
- Jumlah atom C = 5 --> Pentosa
- Jumlah atom C = 6 --> Heksosa
b. Monosakarida berdasarkan struktur molekul :
- Model Fischer
- Model Howarth
c. Contoh Monosakarida :
Monosakarida
|
Komposisi
|
Terdapat dalam
|
Glukosa
|
C6H12O6
|
Buah-buahan
|
Fruktosa
|
C6H12O6
|
Buah-buahan,
Madu
|
Galaktosa
|
C6H12O6
|
Tidak
terdapat secara alami
|
- Disakarida
a. Maltosa
Terbentuk dari 2 molekul glukosa.
" α – D – Glukosa + α – D – Glukosa --> Maltosa + H2O"
Senyawa ini biasa terdapat pada makanan pokok (nasi) dan kecambah biji-bijian.
Ikatan α - 1,4 - Glikosida
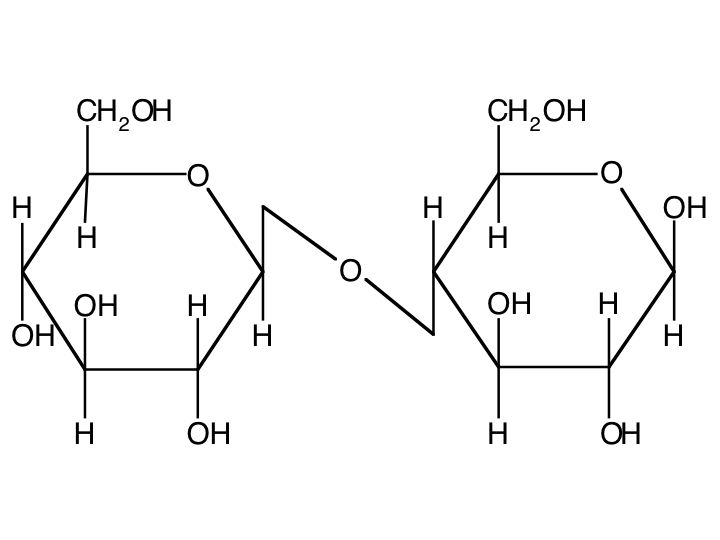
b. Selubiosa
" β – D – Glukosa + α – D – Glukosa --> Selubiosa + H2O "
Senyawa ini biasa terdapat pada tumbuh-tumbuhan seperti serat kayu.
Ikatan β - 1,4 - Glikosida
c. Laktosa
Terbentuk dari molekul glukosa dan galaktosa.
" β – D – Galaktosa + α – D – Glukosa --> Laktosa + H2O "
Senyawa ini biasa terdapat pada susu.
d. Sukrosa
Terbentuk dari molekul glukosa dan fruktosa.
" α – D – Glukosa + α – D – Fruktosa --> Sukrosa + H2O "
Senyawa ini biasa terdapat pada gula tebu, gula bit.
- Polisakarida
a. Amilosa / Amilum (Pati)
Yaitu maltosa yang memanjang. Amilum digunakan sebagai simpanan energi tumbuhan.
b. Amilopektin
 |
| Ikatan α - 1,4 - Glikopiranosa dan cabang 1,6 - Glikopiranosa |
c. Selulosa
Digunakan sebagai serat tumbuhan.
 |
| Ikatan β - 1,4 - Glukopiranosa |
d. Glikogen
Digunakan sebagai simpanan energi hewan. Dan juga biasa disebut dengan gula otot.
C. Uji Karbohidrat
a. Uji Fehling
Uji ini dilakukan untuk menentukan karbohidrat sebagai gula pereduksi atau bukan. Pada uji ini, reaksinya ditunjukkan dengan terbentuknya endapan merah bata.
Uji ini dilakukan untuk menentukan karbohidrat sebagai gula pereduksi atau bukan. Pada uji ini, reaksinya ditunjukkan dengan terbentuknya endapan merah bata.
b. Uji Tollens
Pada karbohidrat, reaksinya akan membentuk endapan perak atau biasa disebut dengan cermin perak.
Pada karbohidrat, reaksinya akan membentuk endapan perak atau biasa disebut dengan cermin perak.
c. Uji Iodium
Uji ini dilakukan untuk membedakan amilum, glikogen, dan selulosa.
Amilum + I2 --> Biru
Glikogen + I2 --> Merah coklat
Selulosa + I2 --> Negatif
e. Uji Benedict
Uji ini dilakukan untuk membedakan amilum, glikogen, dan selulosa.
Amilum + I2 --> Biru
Glikogen + I2 --> Merah coklat
Selulosa + I2 --> Negatif
d. Uji Molish
Pereaksi
Molish adalah α-naftol dalam alcohol 95%. Reaksi ini sangat efektif
untuk uji senyawa-senyawa yang dapat di dehidrasi oleh asam sulfat pekat
menjadi senyawa furfural atau furfural yang tersubtitusi. Seperti
hidroksimetilfurfural. Warna merah ungu yang terasa disebabkan oleh
kondensasi furfural atatu turunannya dengan α-naftol.
Selain dari furfural dapat terkondensasi dengan bermacam-macam senyawa fenol atu amin memberikan turunan yang berwarna. Uji molish adala uji umum untuk karbohidrat walaupun hasilnya bukan merupakan reaksi yang spesifik untuk karbohidrat. Hasil yang negated merupakan petunjuk yang jelas tidak adanya karbohidrat dalam sample.

Selain dari furfural dapat terkondensasi dengan bermacam-macam senyawa fenol atu amin memberikan turunan yang berwarna. Uji molish adala uji umum untuk karbohidrat walaupun hasilnya bukan merupakan reaksi yang spesifik untuk karbohidrat. Hasil yang negated merupakan petunjuk yang jelas tidak adanya karbohidrat dalam sample.

e. Uji Benedict
Uji Benedict berdasarkan pada reduksi dari Cu+2 menjadi Cu+ oleh karbohidrat yang mempunyai gugus aldehid atau ketom bebas. Pereaksi Benedict mengandung CuSO4, Na2CO3
dan Na-sitrat. Pada proses reduksi dalam dalam ssuasana basa biasanya
di tambah zat pengompleks, seperti sitrat untuk mencegah terjadinya
pengendapan CuCO3 dalam larutan natrium bikarbonat. Larutan
tembaga alkalis dapat di reduksi oleh karbohidrat yang mempunyai gugus
aldehid bebas atau monoketo bebas.
Disakarida seperti maltosa dan laktisa dapat mereduksi larutan Benedict karena mempunyai gugus keto bebas. Uji Benedict dapat pula dipakai untuk memperkirakan konsentrasi karbohidrat bebas karena berbagai konsentrasi karbohidrat akan membetikan intensitas warna yang berlainan.
f. Uji Barfoed
Disakarida seperti maltosa dan laktisa dapat mereduksi larutan Benedict karena mempunyai gugus keto bebas. Uji Benedict dapat pula dipakai untuk memperkirakan konsentrasi karbohidrat bebas karena berbagai konsentrasi karbohidrat akan membetikan intensitas warna yang berlainan.
f. Uji Barfoed
Pereaksi
Barfoed merupakan larutan tembaga asetat dalam air yang ditambahkan
asam asetat atau asam laktat. Pereaksi ini digunakan untuk membedakan
monosakarida dan disakarida dengan cara mengontrol kondisi percobaan,
seperti pH dan waktu pemanasan. Senyawa Cu2+ tidak membentuk Cu(OH)2 dalam suasana asam. Jadi Cu2O terbentuk lebih cepat oleh monosakarida dari pada oleh disakarida.
g. Uji Seliwanoff
Uji
Seliwanoff merupakan uji spesifik untuk karbohidrat golongan ketosa.
Uji ini didasrkan atas terjadinya perubahan fruktosa oleh asam klorida
panas menjadi asam levulenat dan 4-hidroksimetil furfural, yang
selanjutnya terjadi kondensasi 4-hidroksimetil furfural dengan
resorsonol (1,3-dihydroksibenzen0 yang dihidrolisa menjadi glukosa dan
fruktosa memberi reaksi positif dengan uji Seliwanoff. Glukosa dan
karbohidrat lain dalam jumlah banyak dapat juga memberi warna yang sama.


PEMBUATAN SENYAWA ESTER BUAH ANGGUR
Untuk membuat senyawa ester, kita dapat mereaksikan asam karboksilat dan alkohol. Berikut adalah cara pembuatan senyawa ester dalam buah anggur.
Silahkan download link dibawah ini :
http://www.4shared.com/file/caSFTY13/ESTER_ANGGUR-SMK_SMAK_MAKASSAR.html?